Forschung nach Alternativ- und Ergänzungsmethoden zu Tierversuchen
Das deutsche Tierschutzgesetz legt fest, dass Tierversuche nur durchgeführt werden dürfen, wenn keine Alternativmethoden genutzt werden können. Die zuständigen Behörden und ihre externen Kommissionen genehmigen einen Tierversuchsantrag nur dann, wenn der Wissenschaftler nachweisen kann, dass sein Forschungsvorhaben nicht ohne Tierversuche auskommt und der zu erwartende Nutzen des Experiments das mögliche Leiden des Tieres ethisch rechtfertigt.
Gegenwärtig sind bereits eine Vielzahl Alternativ- und Ersatzmethoden im Einsatz. Zudem unterstützen und fördern sämtliche Institutionen die Entwicklung und Umsetzung weiterer Alternativmethoden. Dazu zählen unter anderen das Bundesministerium für Bildung und Forschung (BMBF), das Bundesministerium für Ernährung und Landwirtschaft (BMEL) sowie die Deutsche Forschungsgemeinschaft (DFG). Auch die Forschungsinstitute und Wissenschaftler selbst haben ein Interesse daran, neue Alternativ- und Ergänzungsmethoden zu entwickeln. Zum einen aus ethischen Gründen, zum anderen aber auch aus Gründen der Effizienz: Gibt es geeignete Alternativen, sind diese häufig billiger als Tierversuche und in der Regel dauern Experimente an Tieren länger als Experimente, die auf alternative Methoden zurückgreifen.
Zu den etablierten Alternativ- und Ergänzungsmethoden in der Forschung zählen aktuell:
Zellkulturen werden in der Forschung häufig verwendet. Normale Zellkulturen (sogenannte primäre Zellkulturen), die direkt aus einem Gewebe entnommen werden, sind jedoch häufig kurzlebig und die Zellen sterben nach einer gewissen Zeit ab (sogenannte Hayflick-Grenze). Um Zellen dauerhaft in Kultur halten zu können, werden permanente Zellkulturen verwendet (sogenannte immortalisierte Zellen). Diese teilen sich ähnlich einer Krebszelle immer weiter und sind so praktisch unbegrenzt lebensfähig. Permanente Zellkulturen ermöglichen eine Untersuchung ohne Versuchstiere, allerdings ändern diese Zellen bei der Immortalisierung häufig ihre ursprünglichen Eigenschaften. Experimente die in Zellkulturen durchgeführt werden, bezeichnet man auch als in vitro-Experimente – im Gegensatz zu in vivo-Experimenten, die im Organismus gemacht werden.
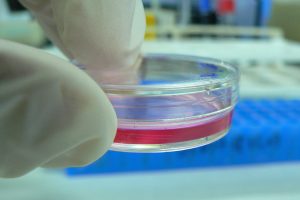
Unterschiedliche Zellen (Muskel, Nerven, Knochen, Haut, Darm, Immunsystem etc.) kommunizieren miteinander und tauschen Informationen aus. Für ihre normale biologische Funktion benötigen Zellen in den meisten Fällen Signale von benachbarten oder auch entfernt liegenden Zellen eines anderen Typs. Um diese Interaktionen zwischen Zellen zu untersuchen, können Forscher verschiedene Zellen gemeinsam kultivieren (sogenannte Co-Kulturen).
Mit solchen Co-Kulturen lassen sich manche biologischen Prozesse im in vitro-Modell nachstellen und bestimmte Tierversuche ersetzen. So kann zum Beispiel beim EPISKIN®-Test die Ätzwirkung von Chemikalien auf einer in der Petrischale gezüchteten menschlichen Epidermis (äußere Hautschicht) untersucht werden. Eine Vielzahl von Tierversuchen wurde dadurch ersetzt.
Bislang ist es aber aus verschiedenen Gründen nicht möglich ganze Organe (Herz, Lunge, Niere, Haut etc.) durch „Züchtung im Reagenzglas“ herzustellen. Für die Medizin von Bedeutung sind aber beispielsweise bereits durch Gewebezüchtung (tissue engineering) hergestellte Gefäßprothesen und Herzklappen.
Für die meisten Experimente ist es im Interesse des Forschers Untersuchungsmethoden zu verwenden, die das Tier nicht oder möglichst wenig belasten. So werden Einflüsse, die das Ergebnis verändern könnten, vermieden. Forscher entwickeln zu diesem Zweck sogenannte nicht-invasive Verfahren, die keinen Eingriff am Tier erfordern. Häufig sind diese innovativen Methoden dann der Ausgangspunkt für die Anwendung solcher Methoden beim Menschen. Beispiele für nicht-invasive Methoden sind moderne bildgebende Verfahren, Atemgasanalysen, oder Messungen von Energiegehalt und Stoffwechselprodukten im Kot oder Urin.
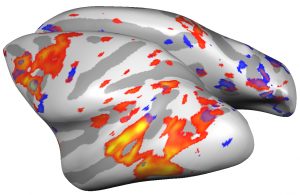
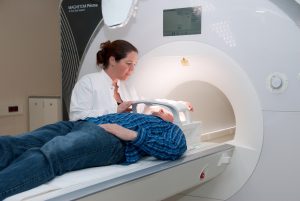
Bildgebende Verfahren: Dieser Bereich hat sich in jüngster Zeit enorm entwickelt und eröffnet vielversprechende Perspektiven. Bildgebende Verfahren wie die Computertomographie (CT) oder die Magnetresonanztomographie (MRT) liefern dreidimensionale Darstellungen von Geweben und Organen – schmerzfrei und in Echtzeit. So können Forscher die Leistungen bestimmter Hirnareale oder das Verhalten von Wirkstoffen bei Gesunden und Patienten beobachten und vergleichen. Experten erwarten, mit Hilfe von bildgebenden Verfahren die Zahl der Versuche und die Belastung für die verwendeten Tiere stark vermindern zu können. Aber nicht alle Fragen der Neurowissenschaft lassen sich mit diesen Verfahren beantworten. So sind Wissenschaftler beispielsweise für die Erforschung der komplexen Funktionen einzelner Nervenzellen im Gehirn oder im Wechselspiel mit dem Hormonsystem nach wie vor auf Tierversuche angewiesen.
Atemgasanalysen: In der ausgeatmeten Luft lassen sich nicht nur die Anteile an Sauerstoff und Kohlendioxid messen. Über die Atemluft gibt der Körper außerdem sogenannte flüchtige organische Moleküle (volatile organic compounds, VOCs) ab, die sich durch neue Methoden der Massenspektrometrie messen lassen. Diese Messmethoden sind so sensibel, dass sie sich auch bei kleinen Nagetieren anwenden lassen. Bestimmte Muster der Zusammensetzung von organischen Molekülen in der Atemluft sind charakteristisch für Stoffwechselfunktionen und Erkrankungen. Bei diesen Untersuchengen müssen die Tiere weder betäubt noch fixiert werden – sie halten sich für die Dauer der Analyse lediglich frei in einem Käfig auf, bei dem die Zu- und Abluft genau kontrolliert wird. Neue Erkenntnisse die bei Untersuchungen an Tieren gewonnen werden und technische Innovationen bei der Weiterentwicklung der Methodik, kommen bei Atemgasanalysen des Menschen zum Einsatz.
Ein Wunschziel der Forscher wäre es, alle Funktionen des Körpers in einem Computermodell simulieren zu können. Daran könnte man dann testen, wie ein neuer Wirkstoff vom Körper aufgenommen und im Stoffwechsel verarbeitet wird. Tierversuche wären dann kaum noch erforderlich. Tatsächlich ist es aber bis heute noch nicht möglich den Zustand auch nur einer einzigen Säugetierzelle zu einem einzigen Zeitpunkt in einem Computer Modell – also in silico – vollständig abzubilden. Dennoch lassen sich inzwischen vereinzelte Organ- und Zellfunktionen am Computer nachbilden. Dadurch können sie unter anderem das Verhalten bestimmter Arzneimittel nachvollziehen – beispielsweise wie lange es dauert, bis der Körper einen Wirkstoff abbaut.
Die Biomedizinische Forschung entwickelt in silico Modelle ständig weiter. Bislang müssen die Beobachtungen am Modell aber immer wieder auch mit Tierversuchen überprüft werden, um zu testen für welche Bereiche die Modelle stimmen und wo die Grenzen sind.
Zu den aktuellen großen Forschungsprojekten aus diesem Bereich zählt das EU-geförderte „Human Brain Project“. Hier arbeiten Wissenschaftler daran, Teile des Gehirns mit computerbasierten Modellen zu simulieren. Ihr Ziel ist es, das Gehirn und seine grundlegenden Funktionen besser zu erforschen. Dadurch könnte in der Zukunft die Zahl der Tierversuche für die Neurowissenschaft reduziert werden.

Beim Microdosing handelt es sich um Experimente am Menschen. Dabei werden freiwilligen Probanden Wirkstoffe in so geringen Mengen verabreicht, dass man davon ausgehen kann, dass sie keinen gesundheitlichen Schaden verursachen sollten. Mit hochempfindlichen Methoden wird dann gemessen, wie sich ein Wirkstoff im Körper bei der Aufnahme, Verteilung, Verstoffwechselung und Ausscheidung der Substanz verhält. Positive oder heilende Effekte auf den Menschen lassen sich beim Microdosing allerdings nicht bestimmen. Neben der ethischen Problematik des Versuchs am Menschen (Hippokratischer Eid und ärztliche Ethik), müssen aber auch die Wirkstoffe die im Microdosing getestet werden zunächst entwickelt werden. Insofern ist das Microdosing eher als erster Schritt vom Versuch im Tier zur Anwendung am Menschen zu verstehen.
Darüber hinaus können Bevölkerungsstudien, Untersuchungen an niederen Organismen wie Bakterien, Pilze oder Hefezellen und durchaus auch an Leichen wichtige wissenschaftliche Erkenntnisse liefern.
Zahlreiche Institutionen unterstützen und fördern die Entwicklung von Alternativ- und Ergänzungsmethoden zu Tierversuchen.
- Das CAAT-Europe (CAAT = Center for Alternatives to Animal Testing) an der Universität Konstanz fördert seit 2009 die Entwicklung von Alternativen zum Tierversuch auf europäischer und transatlantischer Ebene. Es bietet Vertretern aus Industrie, universitärer Forschung, Behörden und Tierschutz die Gelegenheit, sich bei einschlägigen Veranstaltungen über das Thema auszutauschen. Als Vorbild dient das bereits 1981 gegründete CAAT in Baltimore, USA, mit dem eine intensive Zusammenarbeit besteht.
- Das Bundesministerium für Bildung und Forschung (BMBF) unterstützt über 500 Projekte für Alternativmethoden zu Tierversuchen.
- Das Bundesministerium für Ernährung, Landwirtschaft und Verbraucherschutz (BMELV) unterstützt die Entwicklung von Alternativmethoden zu Tierversuchen und verleiht alljährlich seit 2001 den Tierschutzforschungspreis.
- Das Bundesinstitut für Risikobewertung (BfR) in Berlin fördert seit 1990 mehr als 100 Forschungsprojekte und zahlt zirka 35.000 Euro an zehn Arbeitsgruppen für Projekte mit einer Laufzeit von ein bis drei Jahren.
- Die Zentralstelle zur Erfassung und Bewertung von Ersatz- und Ergänzungsmethoden zum Tierversuch (ZEBET) am BfR, 1989 gegründet, überprüft und bewertet die Umsetzung des deutschen Tierschutzgesetzes in der Forschung.
- Ebenfalls beim BfR koordiniert seit September 2015 das Deutsche Zentrum zum Schutz von Versuchstieren (Bf3R) bundesweit die Aktivitäten, um Tierversuche auf ein unerlässliches Maß zu beschränken und den bestmöglichen Schutz der Versuchstiere zu erreichen. Ferner soll das Zentrum die nationale und internationale Forschung sowie den wissenschaftlichen Austausch fördern.
- Die Deutsche Forschungsgemeinschaft (DFG) unterstützt Projekte zur Entwicklung von Alternativmethoden. Sie verleiht regelmäßig den Ursula M. Händel-Tierschutzpreis, unter anderem für die Entwicklung von Alternativmethoden zum Tierversuch. Der Preis ist mit bis zu 100.000 Euro dotiert und wird das nächste Mal am 28.09.2016 verliehen.
- Die Landesregierung von Baden-Württemberg unterstützt die Entwicklung neuer, tierfreier Methoden sowie Forschungsansätze zur Reduzierung der Tierzahlen und der Belastungen für die Tiere mit einem jährlichen Förderprogramm. An der Universität Konstanz ist seit 2006 ein Lehrstuhl für Alternativen zu Tierversuchen eingerichtet.
- Das Ministerium für Umwelt, Forsten und Verbraucherschutz in Rheinland-Pfalz unterstützt die Forschung und vergibt Forschungspreise im Bereich Alternativmethoden zu Tierversuchen.
- An einigen deutschen Universitäten und Hochschulen sind in den vergangenen zehn Jahren Lehrstühle für die Erforschung von Alternativen zu Tierversuchen entstanden. Vorreiter ist seit 2006 der Doerenkamp-Zbinden-Lehrstuhl an der Universität Konstanz unter der Leitung des Toxikologen Prof. Marcel Leist. Er forscht mit seiner wissenschaftlichen Arbeitsgruppe ausschießlich an Zellkulturen und verzichtet komplett auf Tierversuche – bis dato einmalig für einen biomedizinischen Lehrstuhl in Deutschland. In 2016 steigt die Zahl der Professuren für Alternativen zu Tierversuchen und zu deren Verbesserung: Ein Lehrstuhl richtet die Freie Universität in Berlin ein, zwei weitere das Land Hessen in Frankfurt (Alternativen) und in Gießen (Optimierung). Dazu arbeiten weitere universitäre Einrichtungen an der Thematik, zum Beispiel in Tübingen und in Marburg.
- Das Forschungszentrum Jülich unterstützt unter anderem Projekte an Unis und Hochschulen und arbeitet an Konzepten zur Verbreitung von Alternativmethoden wie zum Beispiel Schulungen oder Trainingskurse.
Die Stiftung zur Förderung der Erforschung von Ersatz- und Ergänzungsmethoden zur Einschränkung von Tierversuchen (set) war in zwei Jahrzehnten an über 50 erfolgreich abgeschlossenen Projekten beteiligt. - Das EU-Forschungsprojekt AXLR8 erforscht Alternativen zum Tierversuch zur Giftigkeitsprüfung von Chemikalien und organisiert jährliche Workshops für alternative Teststrategien.
- Die Deutsche Mausklinik (www.mouseclinic.de) entwickelt innovative Methoden der nicht-invasiven Untersuchung von Tiermodellen. Darüberhinaus werden die Tiere von Spezialisten verschiedenster Fachbereich untersucht, um so ein vollständiges Gesamtbild der Krankheit bei den Tieren zu erhalten, das alle Organsystem umfasst. Zusammen mit den anderen Mauskliniken Europas arbeitet der Deutsche Mausklinik im INFRAFRONTIER Verbund an der Verbesserung und Standardisierung von Untersuchungen am präklinischen Tiermodell.
Obwohl zahlreiche Alternativmethoden schon im Einsatz sind, können sie noch nicht sämtliche Tierversuche in der Grundlagenforschung ersetzen. Die meisten Alternativmethoden basieren auf Erkenntnissen, die auf vorherige Tierversuche zurückgehen. Zudem können Alternativmethoden bisweilen häufig nur Teilaspekte der äußerst komplexen Vorgänge im menschlichen Körper simulieren. Aus diesem Grund wird in absehbarer Zeit auf Untersuchungen am lebenden Tier nicht völlig verzichtet werden können.
Zurück zur vorhergehenden Version






